Телеграм канал «ATP Cardiology news | Новости кардиологии»
Для связи: @misterJ_ATP

телеграм-каналов

рекламных размещений, по приросту подписчиков,
ER, количеству просмотров на пост и другим метрикам

и креативы
а какие хуже, даже если их давно удалили

на канале, а какая зайдет на ура

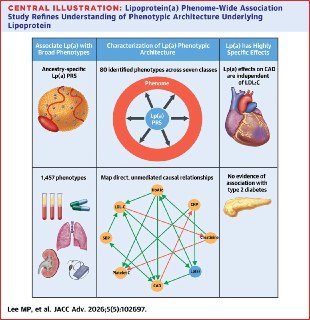
Лп(а) давно в списке подозреваемых по многим сердечно-сосудистым «преступлениям». Но за что он отвечает на самом деле — независимо от холестерина липопротеинов низкой плотности? Менделевское рандомизированное исследование на 425 677 участниках UK Biobank даёт неожиданно чёткий ответ.
Из 1456 изученных фенотипов повышенный Лп(а) оказывал прямое причинное действие, независимое от холестерина липопротеинов низкой плотности, только в двух точках:
— Ишемическая болезнь сердца — отношение шансов 1,36 (95% ДИ: 1,21–1,54) — Гликированный гемоглобин (HbA1c) — умеренное, но значимое повышение
Всё остальное — либо опосредованные эффекты, либо статистический шум.
Про диабет — отдельно. Существовала гипотеза, что очень низкий Лп(а) повышает риск сахарного диабета 2-го типа. Исследование её не подтвердило: связи с диабетом 2-го типа и уровнем HbA1c при низком Лп(а) выявлено не было.
Про пороговые значения — важно для практики. Действующие рекомендации США и Европы называют порог 125/105 нмоль/л. Данное исследование показывает: оптимальная точка для стратификации риска инфаркта миокарда — — у лиц европейского происхождения: 86 нмоль/л (77-й перцентиль) — у лиц африканского происхождения: 93 нмоль/л (59-й перцентиль)
Иными словами, часть пациентов с «нормальным» по текущим руководствам Лп(а) уже находится в зоне повышенного риска.
Вывод для клинициста: Лп(а) — это прицельный удар по коронарному руслу, а не системный яд. Измеряйте его не для галочки, а чтобы найти пациентов, которым снижение именно этого показателя даст наибольший выигрыш.
По материалам: Lee, M, Koenigsberg, S, Anwar, M. et al. Lp(a) Has Specific Effects on Coronary Artery Disease Independent of LDL-C: A Mendelian Randomization Study. JACC Adv. 2026 May, 5 (5) .
08.06.2026 ПН 20:00-22:00 MSK
Всё об аритмиях: синкопальные состояния
https://spb.doctor/i/260608/?erid=2VtzqxcDcVn
Эксперты: Шубик Ю.В., Медведев М.М., Обрезан А.Г.
Реклама. Петербургский Союз Врачей. ИНН 7839069895
Мы знаем, что диабет бьёт по сердцу. Но насколько велик риск именно внезапной сердечной смерти — и сколько лет жизни она забирает? Датское общенациональное исследование даёт конкретные ответы.
Охвачено всё население Дании (2010 год). Из 6862 случаев внезапной сердечной смерти — 97 пациентов с диабетом 1-го типа и 1149 с диабетом 2-го типа.
Риск внезапной сердечной смерти по сравнению с общей популяцией: — Диабет 1-го типа → в 3,7 раза выше — Диабет 2-го типа → в 6,5 раза выше
Оба типа — независимые факторы риска после многофакторной поправки.
Потерянные годы жизни: — Диабет 1-го типа: в среднем 14,2 года (из них 3,4 года — вклад именно внезапной сердечной смерти) — Диабет 2-го типа: 7,9 года (2,7 года — вклад внезапной сердечной смерти)
Неожиданная закономерность: разрыв в риске между диабетиками и здоровыми людьми максимален у молодыхпациентов и уменьшается с возрастом. То есть молодой диабетик — в зоне особого внимания.
Для практики это означает: профилактика внезапной сердечной смерти у пациентов с диабетом — не только удел кардиологов, пациентов высокого риска и пожилых. Молодые пациенты с диабетом заслуживают активной оценки аритмического риска.
По материалам: European Heart Journal, Volume 47, Issue 21, 1 June 2026, Pages 2644–2656
3. Сложность, которая делает документ непригодным для реальной практики.
Сто тридцать четыре страницы. Сорок пять абсолютно новых рекомендаций и восемь пересмотренных — по сравнению с версией 2018 года. При этом за пять лет вышло всего пять крупных РКИ в этой области. Четырнадцать блок-схем ведения, некоторые из них содержат более двадцати стрелок-решений («если — то»). Например, алгоритм для первичной профилактики у взрослых включает 22 разветвления, а схема для диабетиков без сердечно-сосудистых заболеваний — 21.
У американского врача на приём — 10–15 минут. Столь избыточная сложность не просто не помогает, а активно мешает. За множеством целевых уровней холестерина ЛПНП (редко проверенных в РКИ) теряется простое: доказанная польза от статинов проявляется и без этой казуистики.
4. Конфликт интересов как системная проблема.
Даже при формальном соблюдении правил раскрытия конфликта интересов картина удручает. Председатель и заместитель председателя комитета не имеют отраслевых связей, но 16 из 31 члена рабочей группы — имеют. Более двух третей из 29 членов рецензионного совета (призванного независимо оценивать выводы) также раскрыли связи с фармацевтическими, диагностическими, цифровыми и генетическими компаниями.
Но главная проблема даже не в прямом финансовом конфликте, а в интеллектуальной предвзятости. Если вся карьера эксперта построена вокруг методов визуализации, генетического тестирования или цифровых инструментов, он едва ли способен судить о доказательствах за и против этих методов беспристрастно — как «марсианин», по выражению критиков.
РЕЗЮМЕ
Хорошие рекомендации должны быть простыми, доказательными и свободными от предвзятости. Новый документ ACC/AHA не соответствует ни одному из этих критериев. Парадоксальным образом его главная польза — повод задуматься о реформе самого процесса создания руководств, с привлечением независимых авторов и строгим следованием реальным уровням доказательности, а не традиции назначать лечение всё новым группам пациентов.
По материалам Medscape
Новые рекомендации Американского колледжа кардиологии (ACC) и Американской кардиологической ассоциации (AHA) по лечению дислипидемий, призванные помогать врачам, на деле создают иллюзию точности там, где господствует неопределённость. Вместо прагматичного и доказательного документа мы получили громоздкий, внутренне противоречивый и зачастую умозрительный свод правил. Ниже — его четыре главные проблемы.
1. Пропасть между классом рекомендаций и реальной доказательной базой.
Документ содержит 46 рекомендаций высшего, первого класса — то есть того, что «должно быть сделано, и польза значительно превосходит риск». Однако лишь каждая пятая из них опирается на бесспорные данные (уровень А, требующий как минимум двух рандомизированных контролируемых исследований). Почти 40% рекомендаций класса I базируются на уровне доказательности B-NR — иными словами, на нерандомизированных исследованиях, а то и просто на мнении экспертов.
Рассмотрим три примера. Во-первых, оценка коронарного кальция (CAC) у лиц среднего риска — рекомендация класса I, хотя нет ни одного РКИ, которое бы доказало, что такая стратегия снижает твёрдые конечные точки (как смертность). Во-вторых, назначение липидоснижающей терапии при случайной находке кальциноза на КТ, выполненном по другому поводу: здесь нет даже наблюдательных исследований должного качества, что неизбежно ведёт к гипердиагностике и избыточному лечению. В-третьих, однократное измерение липопротеина(а) у всех взрослых с каскадным скринингом родственников — при полном отсутствии доказательств того, что такая тактика улучшает исходы.
2. Искусственное манипулирование порогами риска.
Авторы справедливо предлагают использовать новую модель PREVENT вместо прежней (PCE), так как она точнее калибрована. Логичным следствием этого стало бы уменьшение числа кандидатов на пожизненный приём статинов — ведь PREVENT систематически даёт более низкие оценки риска.
Однако вместо того чтобы честно заключить «статины нужны меньшему числу пациентов», разработчики рекомендаций понижают сам порог «умеренного риска». Если раньше таковым считался 10-летний риск 7,5–20%, то теперь — 5–10%. Формально это обосновывается анализами чистой пользы, но по сути является попыткой сохранить привычное количество пациентов, подлежащих лечению. Возникает резонный вопрос: почему бы просто не сказать пациенту, что статины снижают риск примерно на четверть, а дальше пусть решение принимает он сам, а не многостраничная алгебра рисков?
Продолжение ниже
Абдоминальное ожирение связано с ускоренным биологическим старением по всем показателям, включая метаболомику, клинические биомаркеры и метилирование ДНК. Ускорение биологического старения определяет более высокие риски сердечно-сосудистых заболеваний, смерти и старческой астении. Метаболическое старение объясняло значительную часть этих закономерностей.
Китайские исследователи использовали данные проспективного когортного исследования, чтобы оценить, связано ли абдоминальное ожирение с ускоренным биологическим старением и вносит ли вклад в развитие сердечно-сосудистых и общих возрастных изменений.
В период с 2004 по 2008 год в анализ были включены взрослые в возрасте 30–79 лет, у которых исходо не было сердечно-сосудистых заболеваний. Данные по клиническим биомаркерам, метаболомике и метилированию ДНК были проанализированы у 12 369, 4391 и 980 взрослых соответственно.
Биологические часы возраста были разработаны на основе метаболомики крови (MetaboAge), стандартных клинических биомаркеров и физических показателей (биологический возраст по методу Клемеры – Дубала, KDM-BA), а также метилирования ДНК (DNAm PhenoAge).
Исследователи изучили связь отношения окружности талии к окружности бедер и его варианта, скорректированного по ИМТ, с ускоренным биологическим старением, используя как наблюдательные модели, так и менделевскую рандомизацию.
Оба показателя — MetaboAge и KDM-BA — предсказывали смертность от всех причин точнее хронологического возраста (P < 0,01 для обоих). DNAm PhenoAge не добавил прогностической ценности.
Более высокое отношение окружности талии к окружности бедер и его вариант, скорректированный по ИМТ, были связаны с ускоренным старением. Генетические данные подтвердили потенциальный причинно-следственный эффект. Ускорение MetaboAge и KDM-BA ассоциировалось с повышенным риском атеросклеротических сердечно-сосудистых заболеваний и связанной с ними смертности, а также смертности от всех причин. Ускорение KDM-BA также было связано с повышенным риском старческой астении, тогда как DNAm PhenoAge — только со смертностью от всех причин.
Ускорение MetaboAge опосредовало около 10,5–25,3% связи между отношением окружности талии к окружности бедер и сердечно-сосудистым старением и до 60,6% связи со смертностью от всех причин.
«Полученные данные подчеркивают важность учета распределения жира в исследованиях старения и указывают на потенциал метаболически ориентированных вмешательств для замедления биологического старения у людей с абдоминальным ожирением. Более того, вмешательства, направленные на модуляцию самого процесса старения, могут помочь смягчить неблагоприятные последствия для здоровья, связанные с абдоминальным ожирением, предлагая дополнительную стратегию к традиционным подходам, основанным на изменении образа жизни или контроле веса», — пишут исследователи.
По материалам Medscape Medical News, BMJ
04.06.2026 ЧТ 20:00-22:15 MSK
ХСН и дислипидемия: новые стратегии курации
https://spb.doctor/i/260604/?erid=2Vtzqw9jcYY
Эксперты: Ситникова М.Ю., Обрезан А.Г.
Реклама. Петербургский Союз Врачей. ИНН 7839069895